Tanári útmutató
Autoimmun betegségben szenvedő nők prekoncepcionális és terhesgondozása
(Haladó szint)
2. dia. Határozza meg a tananyag céljait
A terhesség immunológiájának megismerése
Az autoimmun betegségben szenvedő terhes nők speciális csoportjainak megismerése
Az autoimmun betegségben szenvedő nők terhesség alatti kockázatértékelésének lehetővé tétele
Megfelelő terhesség előtti tanácsadás
A konkrét kockázatok és megelőzési módszerek azonosítása
3. dia.
Magyarázza el a nemek közötti különbségeket az autoimmun betegségekkel kapcsolatban.
Az autoimmun betegségek sokkal gyakrabban fordulnak elő nőknél, mint férfiaknál. A genetikai, környezeti és hormonális tényezők kölcsönhatása mind befolyásolja az immunrendszer fejlődését. A férfiak és nők közötti különbségek egyértelműek az autoimmun betegségekre, de a fertőző betegségekre és a ráktípusokra való hajlamukban is.
A nők immunválaszuk számos klinikai jellemzőjében különböznek a férfiaktól.
4. dia
Magyarázza el az autoimmun betegségek epidemiológiáját. A nők gyakrabban szenvednek autoimmun betegségben, mint a férfiak. Ezen a dián néhány autoimmun betegség, például SLE, RA, autoimmun pajzsmirigy betegségek, gyulladásos bélbetegségek, vaszkulitok, autoimmun uveitis előfordulását láthatjuk nemek szerint. Úgy tűnik, hogy a nők hajlamosabbak az autoimmun betegségek kialakulására, mint a férfiak.
5. dia.
A szokásos életkor, amikor a nőknél autoimmun betegséget diagnosztizálnak, gyakran átfedi a fogamzóképes kort. Ez a diagram azt mutatja, hogy a tendenciózus fogamzóképes kor fokozatosan növekszik minden évben, így több nőnek lehet krónikus betegsége a terhesség idején.
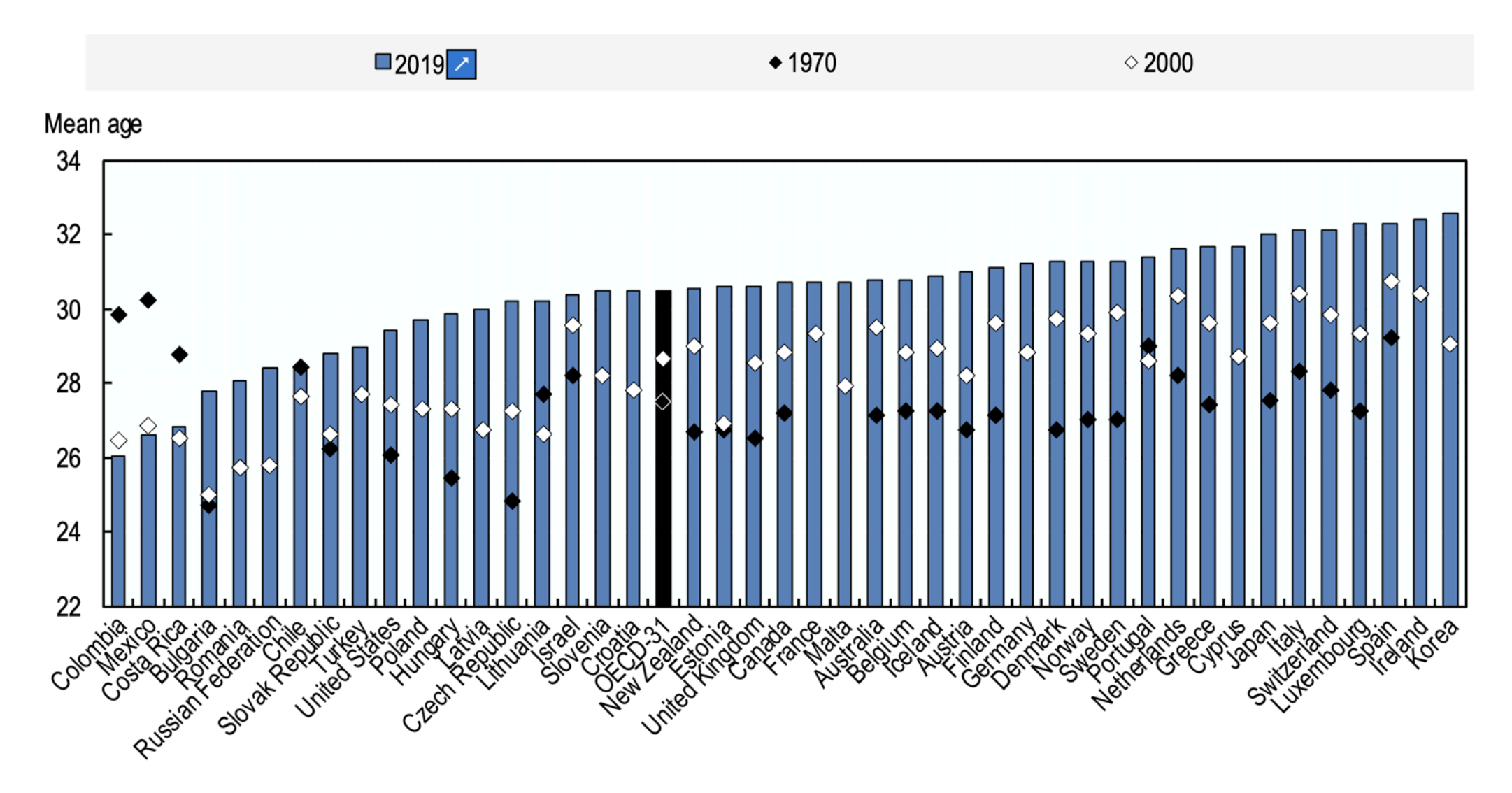
Ez a tendencia a társadalmi attitűdökből és elvárásokból ered, ami veszélyezteti a nők reprodukciós potenciálját. A legtöbb OECD-országban a nők szüléskori átlagéletkora 1970 és 2019 között 2–5 évvel nőtt, a legnagyobb mértékben (5,4 év) Csehországban. Három latin-amerikai ország (Kolumbia, Costa Rica és Mexikó) kivételével, ahol a nők szüléskori átlagéletkora 1970 óta több mint két évvel csökkent.
A nők reproduktív csúcsévei a késő tizenévesek és a 20-as évek vége között vannak. 30 éves korig a termékenység (a teherbe esés képessége) csökkenni kezd. Ez a csökkenés 35 éves koruk elérésekor gyorsabbá válik. 45 éves korára a termékenység annyira csökkent, hogy a legtöbb nő számára valószínűtlen a természetes teherbe esés. A termékenységi szempontokról szóló oktatás fontosnak tűnik a jövő generációja számára, hogy teljes mértékben kiteljesítsék reprodukciós potenciáljukat.
6. dia
Ez egy másik grafikon, amely a 30-as éveik végén szülő nők növekvő számát magyarázza. Látható, hogy a 35 év feletti születések száma 2004 és 2016 között folyamatosan nő, ami azt jelenti, hogy a nők egyre nagyobb hányada lesz szülészeti kockázatnak kitéve megnövekedett életkora és társbetegségei, valamint a mesterséges reprodukciós technikák növekvő használata miatt. Ez nem jelenti azt, hogy maga a termékenység nem csökkent az életkorral!
7. dia
Magyarázza el, miért jelent kockázatot az előrehaladott kor a szülészetben.
Magyarázza el a gyulladásos autoimmun betegségben szenvedő terhes nők speciális magzati és anyai kockázatait.
8. dia
Magyarázza el az immunrendszer alkalmazkodását a semiallogén magzathoz.
11. dia
Milyen változások történnek az immunrendszerben a terhesség alatt? Hogyan befolyásolják ezek a változások az autoimmun betegség aktivitását?
Magyarázza el a terhesség alatti immunológiai változásokat. Eltolódás van a Th1 és Th2 típusú immunválasz között, és a Th2 dominancia jellemzi a terhességet. Ez az immunológiai eltolódás elősegíti a gyulladáscsökkentő citokin funkció előnyben részesítését és ezen keresztül a terhesség fenntartását.
Magyarázza el, hogy az autoimmun betegség hogyan befolyásolhatja a terhességet, és hogyan vezethet az immunológiai chnges az alapul szolgáló autoimmun állapot megváltozásához.
12. dia
Az új immunológiai vizsgálatok kimutatták, hogy a terhesség immunológiai változásainak figyelembe vételekor különbséget kell tennünk a terhesség három fázisa szerint. A gyulladáskeltő mikrokörnyezet elengedhetetlen a normális implantációhoz és szüléshez, míg a toleranciagén környezet a terhesség alatt indukálódik, hogy lehetővé tegye a normális placentációt és a magzati növekedést. A placenta és a decidua helyi immunológiai változásai biztosítják a terhesség sikerét. A decidua citokin profilja a magzati sejtek és hormonok kölcsönhatásának eredménye, és hogy a TH1-TH2 paradigmát egy összetettebb paradigmával kell helyettesíteni, amely magában foglalja a TH1, TH2, TH17 és Treg sejteket.
Az első fázis az implantációtól a korai placentációig tartó időszakot írja le. Ezen a ponton főként veleszületett immunsejtek, például NK-sejtek, dendritikus sejtek, makrofágok, neutrofilek és 3-as típusú veleszületett limfoid sejtek (ILC3-ak) felelősek az IFNγ, IL-1, TNF, IL-6, IL-17 és az IL-6 család citokin leukémia gátló faktorából (LIF) álló inflammatorikus immunmilleuért. Gyulladáskeltő M1 makrofágok, amelyek IL-23-at vagy IL-12-t, valamint LIF-et választanak ki; decidual NK sejtek gyengén citolitikusak, de citokineket és kemokineket termelnek, mint például IFNγ és vaszkuláris endothel növekedési faktor, amelyek elősegítik a spirális artériák átépülését. Ezek a tényezők elengedhetetlenek a sikeres implantációhoz.
A terhesség második szakaszában a feto-anyai felületen történő kilökődés elkerülése érdekében gyorsan fejlődik a tolerogén állapot. Az ösztrogén, a sejtek és a szabályozó fehérjék hatnak a decidual stromális sejtekre és a tolerogén dendritikus sejtekre, kiterjesztik a FOXP3+ Treg sejteket, megváltoztatják a gyorsan növekvő számú természetes gyilkos (NK) sejtek működését és csökkentik az effektor T (Teff) sejteket. A gyulladáscsökkentő citokin termelés nő. Ennek eredményeként a félig allogén magzat tolerálható.
A terhesség harmadik szakaszában - szüléskor - ismét fontos a gyulladáskeltő mikrokörnyezet. A veleszületett immunsejtek, mint például a neutrofilek és a makrofágok beszivárognak a deciduába és a chorioamnion membránokba a vajúdás ideje alatt, és mátrix metalloproteinázokat, IL-1-et, IL-6-ot, TNF-et és nitrogén-oxidot választanak ki.
A fent említett változások mindegyike befolyásolja az autoimmun betegség aktivitását a terhesség alatt. A jól kontrollált autoimmun betegségeknek kisebb az aktivitás kockázata a terhesség alatt, míg az aktív betegség perifoganilag a fellángolás kockázatát jelenti. Ez a jellemző a terhességalatti immunológiai eltolódások jellegében rejlik.
13. dia
Magyarázza el a terhesség és az autoimmun betegségek kölcsönhatását a gyulladásos reumás betegségek (IRD) példáján, amely a különböző autoimmun betegségek nagy csoportja. Ezek a betegségek általában szisztémásak, és így teljes mértékben befolyásolják a betegek immunválaszát.
Az IRD terhességre gyakorolt hatásának megértésével és fordítva extrapolálhatjuk más szisztémás autoimmun betegségek hatását a terhesség lefolyására. Azonban minden egyes autoimmun állapotnak sajátos szempontjai lehetnek a terhességre. Sajnos ez a szeminárium hatóköre nem teszi lehetővé az egyes szisztémás autoimmun betegségek külön megvitatását.
A szisztémás lupus erythematosusra és a reumás arthritisre összpontosítunk, mint az IRD fontos példáira a terhességekben. A szervspecifikus autoimmun betegségek, mint például az M.Basedow, az autoimmun thyreoiditis, az autoimmun hepatitis nem kerülnek megvitatásra.
14. dia
Magyarázza el a terhesség alatti reumás betegséggel kapcsolatos szövődményeket, például fellángolást, szív- és tüdő-, hematológiai, veseproblémákat. Egyes betegeknél szülészeti vagy trombotikus, vagy mindkét szövődmény jelentkezik az antifoszfolipid antitestekkel kapcsolatban, amelyek általában autoimmun betegségekkel járnak.
Magyarázza el a terhességi szövődmények prevalenciáját, mint például a koraszülés, az intrauterin növekedés elmaradása, a preeklampszia fokozódik a reumás betegségekben szenvedő betegeknél.
Magyarázza el az antifoszfolipid antitestszűrésen alapuló kockázatértékelést. Részletezze a szindrómát, annak diagnózisát, kritériumát és a terhesség alatt és azon kívül felmerülő lehetséges kockázatokat.
15. dia
Magyarázza el a prekoncepciós terhességi tanácsadás és tervezés fontosságát ezen dia alapján. Ez a dia az SLE példáján mutatja be, hogy az alapbetegség aktivitása hogyan befolyásolja a terhességi szövődményeket. Láthatjuk, hogy a nagyon aktív autoimmun állapot növeli a terhességi szövődmények kockázatát.
16. dia
Magyarázza el az interdiszciplinaritás értékét az autoimmun betegségben szenvedő terhes nők kezelésében.
A terhesség előtti tanácsadás fontos a módosítható kockázati tényezők felméréséhez, valamint a betegség aktivitásának és terápiájának optimalizálásához a fogamzás előtt.
A terhesség lefolyásának optimalizálása érdekében a következő szempontokat kell figyelembe venni:
Hatékony fogamzásgátló módszereket kell javasolni mindaddig, amíg teratogén gyógyszereket nem adnak, és amíg az alapbetegség kb. 6 hónapig el nem éri a remisszió egyensúlyi állapotát.
A preconceptionális ellátás magában foglalhatja az immunszuppresszív gyógyszerek adaptációját, magában foglalhatja a folsav fokozott szükségességét. A metotrexát-kezelés után vagy a folyamatban lévő szulfaszalazin-kezelés alatt álló betegeknek szignifikánsan magasabb folsavszubsztitúcióra van szükségük (napi 5 mg). A helyettesítést négy-tizenkét héttel a fogamzásgátlás abbahagyása előtt kell elkezdeni. Ezenkívül a folsavbevitelt a terhesség alatt a szupfaszalazin bevitele esetén, a terhesség alatti metotrexát bevitele esetén pedig a terhesség előtti metotrexát bevitele esetén a terhesség teljes időtartama alatt folytatni kell.
Ezenkívül a csontritkulás fokozott kockázata miatt hasznos ellenőrizni a szérum D-vitamin szintjét.
Az oltási státuszt, beleértve az ellenanyagtitereket is, következetesen ellenőrizni kell. A varicella, rubeola, kanyaró, mumpsz elleni nem megfelelő védelem esetén a beteget élő vakcinával kell vakcinázni az immunszuppresszánsok beadása előtt.
A fogamzásgátlást csak az oltás után egy hónappal szabad abbahagyni. Az influenza elleni védőoltás és a szamárköhögés (inaktivált vakcina) mindig ajánlott terhesség alatt, és lehetőség szerint a második trimeszterben kell beadni.
17. dia
Magyarázza el, miért fontos az antitestvizsgálat a gyulladásos autoimmun betegségben szenvedő terhességek kockázatértékelése szempontjából.
18. dia
A sikeres fogantatás előtti tanácsadáshoz elengedhetetlen ennek a szindrómának az időben történő felismerése. Fontosak a trombózis vagy a korábbi terhességi szövődmények, például a koraszülés, a halvaszületés, a méhen belüli növekedés korlátozása, az ismétlődő korai abortuszok vagy a késői abortusz története. Terápiás szempontból az APLAS terhesség alatt kezelhető és kezelhető thrombocyta aggregáció gátlókkal, például ThromboASS-szel® és/vagy alacsony molekulatömegű heparinokkal.
19. dia
Magyarázza el az SSA/SSB antitestek relevanciáját, amelyek az újszülöttkori lupusz fokozott kockázatát jelentik. Az újszülöttkori lupus előfordulási gyakorisága ritka 100 SSA/SSB antitesttel rendelkező beteg közül 2.
20. dia
A Sjögren-szindróma vagy SLE összefüggésében SSA/SSB antitestekkel rendelkező terhes nőknél fennáll a magzati AV-blokk kockázata (kb. 2%). A következő terhességben az ismétlődés kockázata sokkal magasabb, becslések szerint 20%.
Magyarázza el a lehetséges kockázatcsökkentési stratégiákat és az NLE-ben szenvedő gyermekek kimenetelét
21. dia
Ismertesse az SLE szülészeti kockázatait. A kötőszöveti rendellenességek, mint például az SLE és a Sjögren syndrom vagy a kevert kötőszöveti betegségek több szülészeti szövődménysel járhatnak. Ezért a terhesség előtti tanácsadás rendkívül fontos.
Aktív, súlyos SLE-betegség esetén a koraszülések aránya jelentősen, 58 százalékkal nő (szemben a 8 százalék a kontrollcsoportban), valamint egyéb terhességi szövődmények.
22. dia
Magyarázza el, hogy ritka esetekben a terhesség ellenjavallt, mivel a leendő anyát nagy a súlyos szövődmények kockázata. A terhesség ellenjavallt, pulmonális hipertónia, aktív és aktuális neurológiai és vese érintettség esetén, mivel a terhes nők halálozása ebben az esetben 20-szor magasabb.
A betegség enyhe formáiban nincs ellenjavallat a terhességre, azonban a klinikai remissziót a fogamzás előtt hat hónapig kell megcélozni.
23. dia
Beszéljétek meg, hogy a terhességre való felkészülés kulcsfontosságú a kockázatcsökkentéshez.
Magyarázza el a különböző terápiás beavatkozásokat és azok hatását a magzatra.
24. dia
Helyezze kontextusba a veleszületett rendellenességeket és a korai vetélést. Magyarázza el az egészséges terhes nők háttérkockázatait, és tegye ezt a teratogén gyógyszerekkel kapcsolatban. Magyarázza el, hogy a gyógyszeres kezelés mely aspektusai befolyásolják a teratogén potenciált (felezési idő, placentán való átkelés, enzimatikus lebomlás, terhesség hete...)
Szakmai tanácsadásra van szükség abban az esetben, ha ezen terápiák keretében nem szándékos terhesség következik be. A terhesség megszakítása minden esetben egyéni döntés, melynek interdiszciplináris (szülészeti, reumatológiai, embriológiai) részletes tanácsadáson kell alapulnia. Meg kell adni a kezelés abbahagyásának pontos időpontját, a korai vetélés és a veleszületett rendellenességek abszolút és relatív kockázatát.
Amint az ebben a táblázatban látható, a veleszületett rendellenességek és vetélések relatív kockázata a gyógyszeres kezelés nélküli alapkockázathoz képest nagymértékben eltér ezen immunszuppresszív szerek között.
25. dia
Beszélje meg a biztonságos immunmoduláló gyógyszeres lehetőségeket.
26. dia
Mielőtt a regiszter adatai elérhetővé váltak volna, általános volt azt tanácsolni a nőknek, hogy ne szedjenek biológiai gyógyszereket fogantatás, terhesség vagy szoptatás, illetve szoptatás alatt.
A TNF alfa-blokkolókkal terhességet tervező nők gyakori kérdései az újszülött fertőzéseire és az esetleges fejlődési rendellenességekre vonatkoznak. A vizsgálatok nem növelik a fertőzések kockázatát vagy a veleszületett rendellenességek fokozott előfordulási gyakoriságát.
Most már tudjuk, hogy a TNF alfa-blokkolók, mint például a certolizumab és az etanercept alkalmazhatók a terhesség alatt. Más TNF alfa-blokkolók kevesebb adattal rendelkeznek a terhesség alatt, és beadhatók, ha egy adott beteg előnye meghaladja a gyógyszer kockázatát.
27. dia
A magzati immunitást a terhesség alatt az IgG antitesteknek az anyai keringésből a magzati keringésbe történő átvitelével szerezzük meg. Az öt fő antitestosztály közül csak az IgG kerül át a placentán. A köldökzsinórszérumok elemzése kimutatta, hogy minden IgG alosztály átadódik a magzatnak, de az IgG1 preferenciális transzportját találták. A terápiás monoklonális antitestek (mAb-ok) leggyakrabban az IgG1 alosztályba tartoznak, amely a leghatékonyabban jut el a magzatba.
28. dia
A fejlődési toxicitás vizsgálatára használt összes állatfajnál a magzat IgG-expozíciója nagyon alacsony az organogenezis során, de ez a vemhesség második felében növekszik, így az újszülött az anyához hasonló IgG1 koncentrációval születik. Az adatok azt mutatják, hogy az anyai IgG koncentráció a magzati vérben a második trimeszter elejétől a félidőig növekszik, és a legtöbb antitest a harmadik trimeszterben keletkezik. Az első trimeszterben csak maradék mennyiségű IgG1 antitest jut át a placenta gáton. Ezért nincs teratogén hatásuk.
29. dia
A születés után a szerzett IgG antitestek lassan lebomlanak a magzati keringésből a születést követő első 6-12 hónapban.
30. dia
A születés után is fennálló immunmoduláció miatt ezért az élő vírus elleni védőoltással óvatosan kell eljárni. Ez azt jelenti, hogy az élő vakcinákat először 12 hónappal a születés után lehet beadni. Ez befolyásolhatja a BCG, rotavírus és MMR oltásokat.
31. dia
Összefoglalva, tisztában kell lennünk azzal, hogy:
A családtervezéssel minden reproduktív korú autoimmun betegségben szenvedő betegnél foglalkozni kell.
A betegek terhesség és szoptatás előtt/alatt történő kezelésének az anya betegségaktivitásának megelőzésére kell irányulnia, és nem szabad károsítania a magzatot.
A gyermekre gyakorolt gyógyszeres kezelés kockázatát mérlegelni kell a kezeletlen anyai betegség kockázatával szemben a beteg és a gyermek számára.
A gyógyszeres terápiára vonatkozó döntésnek a reumatológus, a nőgyógyász és a beteg közötti interdiszciplináris és részvételen alapuló megállapodáson kell alapulnia.
Views and opinions expressed are however those of the author(s) only and do not necessarily reflect those of the European Union or the Foundation for the Development of the Education System. Neither the European Union nor entity providing the grant can be held responsible for them.



