Leitfaden für Lehrer
Leitfaden für Lehrer


LEITFADEN FÜR LEHRENDE
9. Schwangerschaftsberatung- und Schwangerschaftsbetreuung von Frauen mit Autoimmunerkrankungen
(Basis)
Folie2:
Definieren Sie die Ziele des Lernmaterials:
- Um mehr über die Immunologie der Schwangerschaft zu erfahren.
- Charakterisierung spezieller Gruppen von Schwangeren mit Autoimmunerkrankungen.
- Eine Risikoabschätzung während der Schwangerschaft für Frauen mit Autoimmunerkrankungen vornehmen zu können.
- In der Lage zu sein, eine angemessene Beratung vor der Schwangerschaft in Anspruch zu nehmen.
- Identifizierung spezifischer Risiken und Präventionsmethoden.
Folie3:
Erklären Sie geschlechtsspezifische Unterschiede bei Autoimmunerkrankungen.
Autoimmunerkrankungen treten bei Frauen weitaus häufiger auf als bei Männern. Das Zusammenspiel von genetischen, umweltbedingten und hormonellen Faktoren beeinflusst die Entwicklung des Immunsystems. Die Unterschiede zwischen Männern und Frauen sind deutlich in ihrer Anfälligkeit für Autoimmunerkrankungen, aber auch für Infektionskrankheiten und Krebsarten. Frauen unterscheiden sich von Männern in mehreren klinischen Merkmalen ihrer Immunantwort.
Folie4:
Erklären Sie die Epidemiologie von Autoimmunerkrankungen.
Frauen leiden häufiger an Autoimmunerkrankungen als Männer. Auf dieser Folie können wir die Häufigkeit einiger Autoimmunerkrankungen sehen, wie SLE, RA, Autoimmunerkrankungen der Schilddrüse, entzündliche Darmerkrankungen, vaskuläre Autoimmunerkrankungen und autoimmune Uveitis nach Geschlecht. Frauen scheinen anfälliger für die Entwicklung von Autoimmunerkrankungen zu sein als Männer.
Folie5:
Das übliche Alter, in dem eine Autoimmunerkrankung bei Frauen diagnostiziert wird, überschneidet sich oft mit dem gebärfähigen Alter. Diese Grafik zeigt, wie das Gebäralter tendenziell von Jahr zu Jahr allmählich ansteigt, sodass mehr Frauen zum Zeitpunkt der Schwangerschaft an chronischen Krankheiten leiden können (Diagramm: OECD-Familien-Datenbank, oe.cd/fdb).
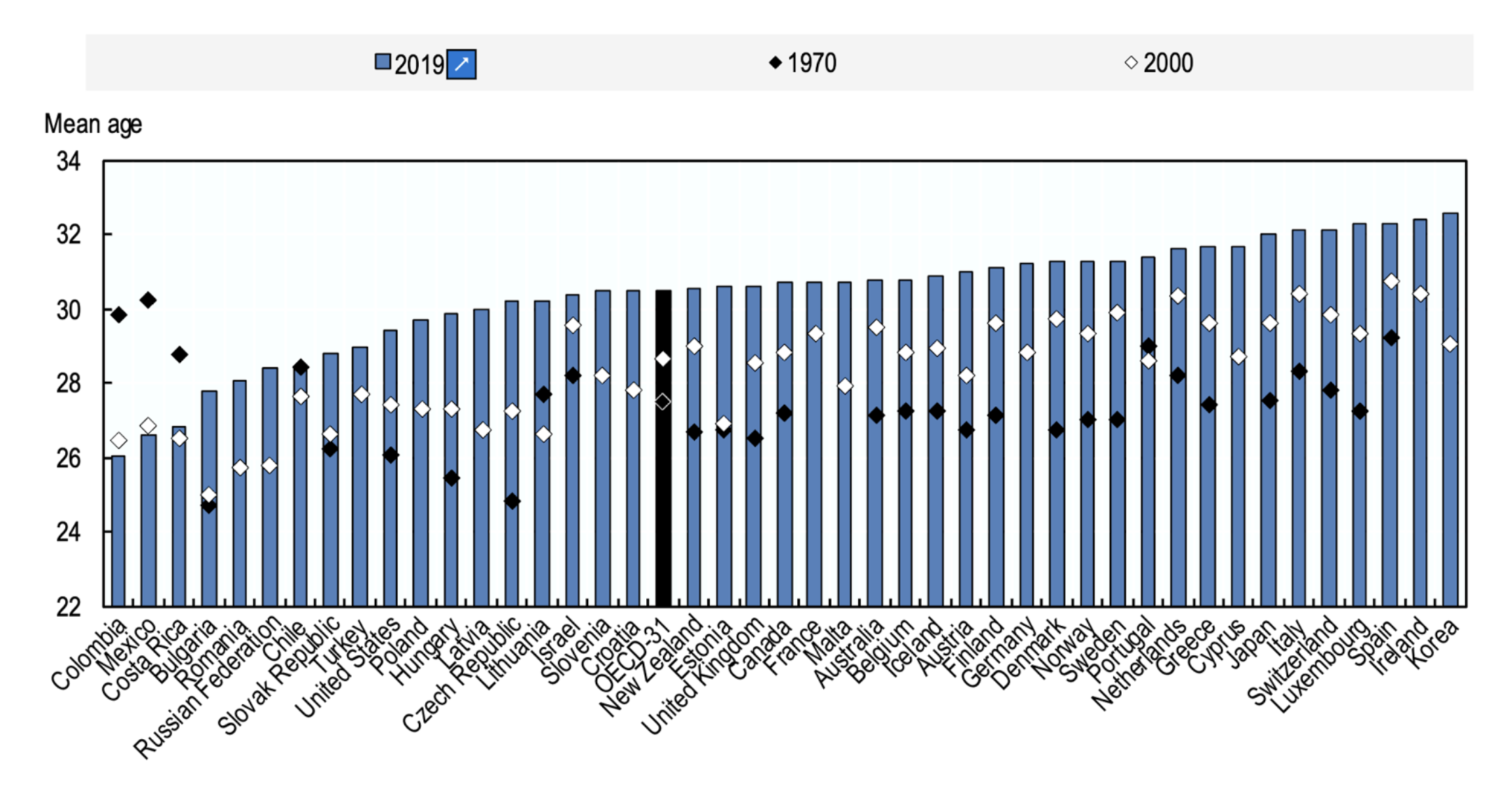
Dieser Trend hat seinen Ursprung in gesellschaftlichen Einstellungen und Erwartungen, die das Fortpflanzungspotenzial von Frauen gefährden. In den meisten OECD-Ländern ist das Durchschnittsalter der Frauen bei der Geburt zwischen 1970 und 2019 um 2 bis 5 Jahre gestiegen, wobei der größte Anstieg (5,4 Jahre) in der Tschechischen Republik zu verzeichnen ist. Mit Ausnahme von drei lateinamerikanischen Ländern (Kolumbien, Costa Rica und Mexiko), in denen das Durchschnittsalter der Frauen bei der Geburt seit 1970 um mehr als zwei Jahre gesunken ist.
Die besten reproduktiven Jahre einer Frau liegen zwischen den späten Teenagern und den späten 20ern. Im Alter von 30 Jahren beginnt die Fruchtbarkeit (die Fähigkeit, schwanger zu werden) abzunehmen. Dieser Rückgang beschleunigt sich, wenn sie das 35. Lebensjahr erreichen. Mit 45 Jahren ist die Fruchtbarkeit so stark zurückgegangen, dass es für die meisten Frauen unwahrscheinlich ist, auf natürliche Weise schwanger zu werden. Die Aufklärung über die Fertilitätsaspekte scheint für zukünftige Generationen wichtig zu sein, um ihr Fortpflanzungspotenzial auszuschöpfen.
Folie6:
Dies ist eine weitere Grafik, die die steigende Zahl von Frauen erklärt, die mit Ende 30 gebären. Sie zeigt, dass die Zahl der Geburten über 35 Jahren zwischen 2004 und 2016 stetig zunimmt, was bedeutet, dass ein zunehmender Anteil der Frauen aufgrund ihres höheren Alters und ihrer Begleiterkrankungen sowie aufgrund des zunehmenden Einsatzes künstlicher Reproduktionstechniken ein geburtshilfliches Risiko haben wird. Dies bedeutet jedoch nicht, dass die Fruchtbarkeit selbst nicht mit dem Alter abgenommen hat!
Folie7:
Erklären Sie, warum ein fortgeschrittenes Alter ein Risiko in der Geburtshilfe darstellt. Erläutern Sie die besonderen fetalen und mütterlichen Risiken von Schwangeren mit entzündlichen Autoimmunerkrankungen.
Folie8:
Erklären Sie die Anpassung des Immunsystems an den semiallogenen Fötus.
Folie11:
Welche Veränderungen passieren im Immunsystem in der Schwangerschaft? Wie beeinflussen diese Veränderungen die Aktivität der Autoimmunerkrankung?
Erklären Sie die immunologischen Veränderungen während der Schwangerschaft. Es gibt eine Verschiebung zwischen der Immunantwort vom Th1- und Th2-Typ, und die Th2-Dominanz kennzeichnet die Schwangerschaft. Diese immunologische Verschiebung trägt dazu bei, die entzündungshemmende Zytokinfunktion und damit die Aufrechterhaltung der Schwangerschaft zu bevorzugen.
Erklären Sie, wie die Autoimmunerkrankung die Schwangerschaft beeinflussen kann und wie die immunologischen Veränderungen zu Veränderungen der zugrunde liegenden Autoimmunerkrankung führen können.
Folie12:
Neue immunologische Studien haben gezeigt, dass bei der Betrachtung der immunologischen Veränderungen in der Schwangerschaft nach den drei Phasen der Schwangerschaft unterschieden werden muss. Eine entzündungsfördernde Mikroumgebung ist entscheidend für eine normale Einnistung und Geburt, während eine tolerogene Umgebung im Laufe der Schwangerschaft induziert wird, um eine normale Plazentation und ein normales Wachstum des Fötus zu ermöglichen. Die lokalen immunologischen Veränderungen der Plazenta und der Dezidua sorgen für den Erfolg einer Schwangerschaft. Das Zytokinprofil an der Dezidua ist das Ergebnis des Zusammenspiels von fetalen Zellen und Hormonen, und das TH1-TH2-Paradigma sollte durch ein komplexeres Paradigma ersetzt werden, das TH1-, TH2-, TH17- und Treg-Zellen umfasst.
Die erste Phase beschreibt den Zeitraum von der Einnistung bis zur frühen Plazentation. Zu diesem Zeitpunkt sind hauptsächlich angeborene Immunzellen wie NK-Zellen, dendritische Zellen, Makrophagen, Neutrophile und Typ 3 angeborene lymphatische Zellen (ILC3s) für das proinflammatorische Immunmilieu verantwortlich, das aus IFNγ, IL-1, TNF, IL-6, IL-17 und dem Zytokin der IL-6-Familie Leukämie-inhibitorischer Faktor (LIF) besteht. Proinflammatorische M1-Makrophagen, die IL-23 oder IL-12 sowie LIF sezernieren; deziduale NK-Zellen sind wenig zytotoxisch, produzieren aber Zytokine und Chemokine, wie IFNγ und vaskulären endothelialen Wachstumsfaktor, die den Umbau der Spiralarterie fördern. Diese Faktoren sind essentiell für eine erfolgreiche Implantation.
Um eine Abstoßung an der feto-maternalen Schnittstelle zu vermeiden, entwickelt sich in der zweiten Phase der Schwangerschaft schnell ein tolerogener Zustand. Östrogen, Zellen und regulatorische Proteine wirken auf deziduale Stromazellen und tolerogene dendritische Zellen, erweitern FOXP3+ Treg-Zellen, verändern die Funktion der schnell steigenden Anzahl von natürlichen Killerzellen (NK) und regulieren Effektor-T-Zellen (Teff-Zellen) herunter. Die entzündungshemmende Zytokinproduktion nimmt zu. Infolgedessen wird der semiallogene Fötus toleriert.
Im dritten Stadium der Schwangerschaft – bei der Geburt – ist wiederum eine entzündungsfördernde Mikroumgebung entscheidend. Angeborene Immunzellen wie Neutrophile und Makrophagen infiltrieren während der Wehen die Dezidua und die Chorioamnionmembran und sezernieren Matrix-Metalloproteinasen, IL-1, IL-6, TNF und Stickstoffmonoxid.
Folie12:
Alle oben genannten Veränderungen wirken sich auf die Aktivität der Autoimmunerkrankung während der Schwangerschaft aus. Gut kontrollierte Autoimmunerkrankungen haben ein geringeres Risiko für Aktivität während der Schwangerschaft, während aktive Erkrankungen perikonzeptionell ein Risiko für einen Schub darstellen. Dieses Merkmal liegt in der Natur der immunologischen Verschiebungen während der Schwangerschaft.
Folie13:
Erläutern Sie das Zusammenspiel von Schwangerschaft und Autoimmunerkrankungen am Beispiel der entzündlich-rheumatischen Erkrankungen (IRD), die eine große Gruppe verschiedener Autoimmunerkrankungen darstellen. Diese Erkrankungen sind in der Regel systemisch und wirken sich somit auf die Immunantwort der Patienten in ihrer Gesamtheit aus.
Indem wir die Wirkung von IRD auf die Schwangerschaft und umgekehrt verstehen, können wir den Einfluss anderer systemischer Autoimmunerkrankungen auf den Verlauf der Schwangerschaft extrapolieren. Jede einzelne Autoimmunerkrankung kann jedoch spezifische Aspekte der Schwangerschaft haben. Leider ist es im Rahmen des Seminars nicht möglich, jede systemische Autoimmunerkrankung separat zu behandeln. Wir werden uns auf systemischen Lupus erythematodes und rheumatische Arthritis als wichtige Beispiele für IRD in Schwangerschaften konzentrieren. Organspezifische Autoimmunerkrankungen wie M. Basedow, Autoimmunthyreoiditis und Autoimmunhepatitis werden hier nicht behandelt.
Folie14:
Erläutern Sie die Komplikationen im Zusammenhang mit der zugrunde liegenden rheumatischen Erkrankung während der Schwangerschaft, wie z. B. Schübe, Herz-, Lungen-, hämatologische und Nierenprobleme. Bei einigen Patientinnen treten geburtshilfliche oder thrombotische Komplikationen oder beides auf, die mit Antiphospholipid-Antikörpern zusammenhängen, die häufig mit Autoimmunerkrankungen in Verbindung gebracht werden.
Erklären Sie die Prävalenz von Schwangerschaftskomplikationen, wie Frühgeburt, intrauterine Wachstumseinschränkung und für das Schwangerschaftsalter kleine Neugeborene. Präeklampsie ist bei Patienten mit rheumatischen Erkrankungen ebenfalls häufiger.
Erläutern Sie die Risikobewertung auf der Grundlage eines Antiphospholipid-Antikörper-Screenings. Erläutern Sie das Syndrom, seine Diagnosekriterien und mögliche Risiken während der Schwangerschaft.
Folie15:
Erläutern Sie anhand dieser Folie die Bedeutung der Schwangerschaftsberatung und -planung vor der Empfängnis. Diese Folie zeigt am Beispiel des SLE, wie sich die Aktivität der zugrundeliegenden rheumatischen Erkrankung auf Schwangerschaftskomplikationen auswirkt. Wir können sehen, dass eine hochaktive Autoimmunerkrankung das Risiko von Schwangerschaftskomplikationen erhöht.
Folie16:
Erläutern Sie den Wert der interdisziplinären Zusammenarbeit bei der Behandlung von schwangeren Frauen mit Autoimmunerkrankungen.
Eine Beratung vor der Schwangerschaft ist wichtig, um modifizierbare Risikofaktoren zu beurteilen und die Krankheitsaktivität und -therapie vor der Empfängnis zu optimieren.
Folgende Punkte sollten beachtet werden, um den Verlauf der Schwangerschaft zu optimieren:
Risikomodifikation durch angemessene Gewichtskontrolle, gesunde und ausgewogene Ernährung und Nikotinabstinenz.
Überprüfung und Änderung der Medikation.
Risikobewertung auf der Grundlage der Krankheitsaktivität, des Antikörperprofils und der geburtshilflichen Vorgeschichte.
Wirksame Verhütungsmethoden sollten vorgeschlagen werden, bis keine teratogenen Medikamente mehr verabreicht werden und bis die zugrunde liegende Autoimmunerkrankung einen stabilen Zustand der Remission für ca. 6 Monate erreicht.
Die Schwangerschaftsvorsorge kann die Anpassung der immunsuppressiven Medikamente beinhalten und einen erhöhten Bedarf an Folsäure mit sich bringen. Patienten nach Methotrexat-Therapie oder unter laufender Sulfasalazin-Therapie benötigen eine signifikant höhere Folsäuresubstitution (5 mg täglich). Die Substitution sollte vier bis zwölf Wochen vor dem Absetzen der Empfängnisverhütung beginnen. Darüber hinaus sollte die Folsäurezufuhr während der gesamten Schwangerschaft bei Sulfasalazin-Einnahme während der Schwangerschaft und in den ersten 13 Schwangerschaftswochen bei Methotrexat-Einnahme vor der Schwangerschaft fortgesetzt werden.
Darüber hinaus ist es aufgrund des erhöhten Risikos für Osteoporose sinnvoll, den Vitamin-D-Spiegel im Serum zu überprüfen.
Der Impfstatus, einschließlich der Antikörpertiter, sollte konsequent überprüft werden. Bei unzureichendem Schutz gegen Varizellen, Röteln, Masern und Mumps sollte der Patient mit einem Lebendimpfstoff geimpft werden, bevor er Immunsuppressiva erhält. Die Empfängnisverhütung darf erst einen Monat nach der Impfung abgebrochen werden. Die Grippeimpfung und Keuchhusten (Totimpfung) werden während der Schwangerschaft immer empfohlen und sollten möglichst im zweiten Trimester verabreicht werden.
Folie17:
Welche Antikörper stellen ein erhebliches Risiko für eine Schwangerschaft dar? Erläutern Sie, warum Antikörpertests für die Risikobewertung bei Schwangerschaften mit entzündlichen Autoimmunerkrankungen relevant sind. Sprechen Sie insbesondere Antiphospholipid-Antikörper und SSA- und SSB-Antikörper an. Erläutern Sie, wie die Krankheitsaktivität aus klinischen und Laborwerten extrapoliert werden kann (z. B. Abnahme des Komplements oder Erhöhung des dsDNA-Antikörpers bei Lupus).
Folie18:
Für eine erfolgreiche präkonzeptionelle Beratung ist es entscheidend, dieses Syndrom rechtzeitig zu erkennen. Fragen zu einer Thrombose in der Vorgeschichte oder zu früheren Schwangerschaftskomplikationen wie Frühgeburten, Totgeburten, intrauterinen Wachstumseinschränkungen, wiederkehrenden Frühaborten oder Spätaborten sind wichtig. Therapeutisch kann und sollte APLAS in der Schwangerschaft mit Thromboaggregationshemmern wie ThromboASS® und/oder niedermolekularen Heparinen behandelt werden.
Folie19:
Erläutern Sie die Relevanz von SSA/SSB-Antikörpern, die ein erhöhtes Risiko für neonatalen Lupus darstellen. Die Inzidenz von neonatalem Lupus ist selten (2 von 100 Patientinnen mit SSA/SSB-Antikörpern).
Folie20:
Schwangere Frauen mit SSA/SSB-Antikörpern im Zusammenhang mit dem Sjögren-Syndrom oder SLE haben ein Risiko (ca. 2 %) für einen fetalen AV-Block. In einer anschließenden Schwangerschaft ist das Rezidivrisiko mit geschätzten 20 % deutlich höher.
Erläutern Sie mögliche Strategien zur Risikominderung und die Ergebnisse von Kindern mit NLE. Befassen Sie sich mit der Verwendung von Hydroxychloroquin zur Risikominderung.
Folie21:
Erläutern Sie die geburtshilflichen Risiken des SLE. Bindegewebserkrankungen wie SLE und Sjögren-Syndrom oder gemischte Bindegewebserkrankungen können mit mehr geburtshilflichen Komplikationen einhergehen. Aus diesem Grund ist eine Beratung vor der Schwangerschaft von größter Bedeutung.
Bei einer aktiven schweren Erkrankung mit SLE ist die Frühgeburtenrate mit 58 % signifikant erhöht (vs. 8 % in der Kontrollgruppe) sowie andere Schwangerschaftskomplikationen.
Folie22:
Erklären Sie, dass in seltenen Fällen eine Schwangerschaft kontraindiziert ist, da sie die werdende Mutter einem hohen Risiko für schwere Komplikationen aussetzt. Eine Schwangerschaft ist kontraindiziert bei pulmonaler Hypertonie sowie aktiver neurologischer und renaler Beteiligung, da die Sterblichkeit von Schwangeren in diesem Fall 20-fach höher ist.
Bei milden Formen der Krankheit gibt es keine Kontraindikation für eine Schwangerschaft, jedoch sollte eine klinische Remission sechs Monate vor der Empfängnis angestrebt werden.
Folie23:
Besprechen Sie, dass die Vorbereitung auf eine Schwangerschaft der Schlüssel zur Risikominderung ist. Erläutern Sie die verschiedenen therapeutischen Interventionen und ihre Wirkung auf den Fötus.
Folie24:
Stellen Sie angeborene Fehlbildungen und frühe Fehlgeburten in einen Kontext. Erläutern Sie die Hintergrundrisiken bei gesunden Schwangeren und setzen Sie diese in Relation zu den teratogenen Medikamenten. Erklären Sie, welche Aspekte eines Medikaments das teratogene Potenzial beeinflussen (Halbwertszeit, Plazentadurchquerung, enzymatischer Abbau, Schwangerschaftswoche).
In der Situation, in der es im Rahmen dieser Therapien zu einer ungewollten Schwangerschaft kommt, ist eine professionelle Beratung erforderlich. Es ist immer eine individuelle Entscheidung für einen Schwangerschaftsabbruch, die auf einer interdisziplinären (Geburtshilfe, Rheumatologie, Embryologie) ausführlichen Beratung beruhen muss. Der genaue Zeitpunkt des Absetzens, das absolute und relative Risiko einer frühen Fehlgeburt und angeborener Fehlbildungen müssen angegeben werden.
Wie in dieser Tabelle zu sehen ist, variieren die relativen Risiken für angeborene Fehlbildungen und Fehlgeburten im Vergleich zum Basisrisiko ohne Medikamente stark zwischen diesen Immunsuppressiva.
Folie25:
Besprechen Sie sichere immunmodulatorische Medikamentenoptionen.
Folie26:
Bevor die Registerdaten verfügbar wurden, war es üblich, Frauen generell von der Einnahme von Biologika während der Empfängnis, Schwangerschaft, Stillzeit oder Stillzeit abzuraten.
Erklären Sie, dass Registerdaten wichtig sind, um Informationen über die Einnahme von Medikamenten in der Schwangerschaft zu sammeln.
Häufige Fragen von Frauen, die eine Schwangerschaft mit Immunsuppressiva planen, betreffen Infektionen des Neugeborenen und mögliche Fehlbildungen.
Studien zeigen kein erhöhtes Risiko für Infektionen oder eine erhöhte Inzidenz von angeborenen Fehlbildungen bei vielen der immunmodulatorischen Medikamente.
Einige der immunmodulatorischen Medikamente können verabreicht werden, wenn der Nutzen bei einem bestimmten Patienten das Risiko des Medikaments überwiegt. Seien Sie sich bewusst, dass ein stabiler Krankheitsverlauf der Schlüssel zur Risikominderung ist.
Folie27-30:
Besprechen Sie anhand des auf Folie 27 beschriebenen Falles den individuellen Aspekt des ratsuchenden Patienten. Schätzen Sie die möglichen realistischen Risiken ein, gehen Sie auf die unrealistischen Ängste ein und versuchen Sie, die Studierenden und ihre Beratungsvorschläge in dieses Gespräch einzubeziehen.
Folie27:
Zusammenfassend müssen wir uns darüber im Klaren sein, dass:
Familienplanung sollte bei jedem Patienten mit Autoimmunerkrankungen im gebärfähigen Alter angegangen werden.
Die Behandlung von Patientinnen vor/während der Schwangerschaft und Stillzeit sollte darauf abzielen, die Krankheitsaktivität bei der Mutter zu verhindern und den Fötus nicht zu schädigen.
Das Risiko einer medikamentösen Therapie für das Kind sollte gegen das Risiko einer unbehandelten mütterlichen Erkrankung für die Patientin und das Kind abgewogen werden.
Die Entscheidung über eine medikamentöse Therapie sollte auf einer interdisziplinären und partizipativen Abstimmung zwischen Rheumatologen, Gynäkologen und Patientinnen beruhen.





